化学作为高考必考课目,占比分数份额也是相对比较大。相信很多孩子在化学的考试过程中,无论是解题思路和技巧都存在或多或少的差异,因此君翰教育作为K12教育领头军,在课外一对一辅导的过程中,结合当前考点、课程同步一对一让孩子将知识点精准掌握
让孩子不再为高中化学考试而烦恼。那么接下来就由君翰教育化学一对一辅导组分享从高一到高三的化学解题技巧和方法。
高一习题
已知X、Y均为有刺激性气味的气体,且几种物质间有以下转化关系,部分产物未标出。请回答下列问题。
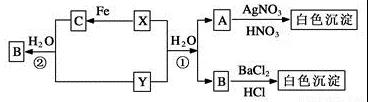

(1)写出下列各物质的化学式:X______、Y______、C______。
(2)反应①的化学方程式为______,反应②的离子方程式为______。
(2)Cl2+SO2+2H2O=2HCl+H2SO4,2Fe3++SO2+2H2O=2Fe2++SO42-+4H+。
【解析】
(1)首先拿到题以后,我们能分析出A和硝酸酸化的硝酸应发生生成白色沉淀,说明A中含有Cl-,B与盐酸酸化的BaCl2反应生成白色沉淀,B中含有SO42-,X、Y均为刺激性气味的气体,因此推出X和Y为Cl2、SO2,X和Fe发生反应,因此可以推断出X为Cl2,Y为SO2,
即C为FeCl3;
即C为FeCl3;
(2)紧接着我们看反应①利用氯气的氧化性,把SO2氧化成SO42-,本身被还原成Cl-,因此离子反应方程式为:Cl2+SO2+2H2O=2HCl+H2SO4,反应②利用Fe3+的强氧化性,把SO2氧化成SO42-,本身被还原成Fe2+,即反应②的离子反应方程式为2Fe3++SO2+
2H2O=2Fe2++SO42-+4H+。
2H2O=2Fe2++SO42-+4H+。
【答案】
(1)Cl2;SO2;FeCl3;
(2)Cl2+SO2+2H2O=2HCl+H2SO4,2Fe3++SO2+2H2O=2Fe2++SO42-+4H+。
【总结】
要细心读题,熟悉各元素的属性、以及反应产生的现象,最后结合题目做出推断。
那么高一化学类型复习题就以此案例来作解答,后续任老师会一一将各类典型题目解题方法和技巧分享出来,那么进入高二化学复习,继续看题。
要细心读题,熟悉各元素的属性、以及反应产生的现象,最后结合题目做出推断。
那么高一化学类型复习题就以此案例来作解答,后续任老师会一一将各类典型题目解题方法和技巧分享出来,那么进入高二化学复习,继续看题。
高二习题
下图是教材中实验装置。
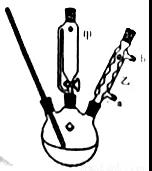

回答下列问题:
(1)甲仪器的名称是______,与同类仪器相比其优点是______、______。
(1)甲仪器的名称是______,与同类仪器相比其优点是______、______。
(2)向乙通水,进水口是_______(填“a”或“b”),理由是_______。
(3)利用上述装置进行醇与酸的酯化反应。
①醇、酸、酯和水之间的沸点满足的条件是_______。
②如果外接一个装置可以满足蒸馏的条件,那么,此时醇、酸、酯和水之间的沸点满足的条件是_______。
(2)a 有利于向上排出空气,使水充满球形冷凝管
(3)①酯的沸点高于其他物质,且有机物易挥发 ②酯的沸点最低或者水的沸点最高
【总结】
在日常做题时 要对各个仪器的特点以及实验原理清楚,并能熟记于心。
【解析】
(1)在化学仪器的使用和辨认上,我们不难发现甲仪器的名称恒压分液漏斗,与同类仪器相比其优点是可以保持三颈烧瓶与分液漏斗的压强相等,利于液体滴入;避免甲中液体散入到空气中。
(2)向乙通水,冷凝水低进高出有利于向上排出空气,使水充满球形冷凝管。
(3)利用上述装置进行醇与酸的酯化反应。
①为了不让酯挥发,醇、酸、酯和水之间的沸点满足的条件是酯的沸点高于其他物质,且有机物易挥发。
①为了不让酯挥发,醇、酸、酯和水之间的沸点满足的条件是酯的沸点高于其他物质,且有机物易挥发。
②如果外接一个装置,为让酯挥发出来,此时醇、酸、酯和水之间的沸点满足的条件是酯的沸点最低或者水的沸点最高。
解析:(1)根据图示,甲仪器的名称分液漏斗,与同类仪器相比其优点是可以保持三颈烧瓶与分液漏斗的压强相等,利于液体滴入;避免甲中液体散入到空气中。
(2)向乙通水,冷凝水低进高出有利于向上排出空气,使水充满球形冷凝管,向乙通水,进水口是a。
(3)①利用上述装置进行醇与酸的酯化反应,为了不让酯挥发,醇、酸、酯和水之间的沸点满足的条件是酯的沸点高于其他物质,且有机物易挥发。
②利用上述装置进行醇与酸的酯化反应,如果外接一个装置,为让酯挥发出来,此时醇、酸、酯和水之间的沸点满足的条件是酯的沸点最低或者水的沸点最高。
【答案】
【答案】
(1)分液漏斗 可以保持三颈烧瓶与分液漏斗的压强相等,利于液体滴入 避免甲中液体散入到空气中
(2)a 有利于向上排出空气,使水充满球形冷凝管
(3)①酯的沸点高于其他物质,且有机物易挥发 ②酯的沸点最低或者水的沸点最高
【总结】
在日常做题时 要对各个仪器的特点以及实验原理清楚,并能熟记于心。
从高一到高二,我们能明显的发现,从开始熟悉各元素的特性到实验室里的实践,最大的感触就是从理论走向了实践,这也在提醒我们同学,课堂上不仅仅要熟知理论,课外也要加强实践,理论与实践相结合才能将知识点灵活运用。高一的基础,高二的实践,接下
来让我们走进高三的灵活运用。
实践,
高三习题
把锌片和铁片放在盛有稀食盐水和酚酞混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,首先观察到溶液变红的区域是( )
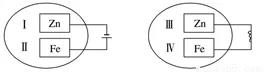

A. Ⅰ和Ⅲ附近 B. Ⅰ和Ⅳ附近
C. Ⅱ和Ⅲ附近 D. Ⅱ和Ⅳ附近
【解析】第一个图示是电解池,铁做阳极,铁失电子生成亚铁离子,锌做阴极,在阴极上,2H++2e-=H2↑,破坏了锌片附近水的电离平衡,使得OH-浓度增大,所以Ⅰ处也变红;第二个图示是原电池,锌做负极,锌失电子形成锌离子,正极是Ⅳ,在正极上,
O2+2H2O+4e-=4OH-;所以Ⅳ处变红;答案选B。
【答案】B
【总结】 高一和高二是打基础环节,高三注重的运用,因此平时要做好总结,归纳,节省答题时间,整理好自己的答题技巧库,诸如此类的题要在最短的时间做出选择。
君翰教育高中化学一对一辅导复习资料今天暂时到这,后面会根据班课反应情况,继续为正在备考的学生分享答题技巧和解题思路。
更多关于高中化学辅导请关注
君翰教育官方网站:www.junhanedu.com
君翰教育高中化学辅导电话:400-8940-050
O2+2H2O+4e-=4OH-;所以Ⅳ处变红;答案选B。
【答案】B
【总结】 高一和高二是打基础环节,高三注重的运用,因此平时要做好总结,归纳,节省答题时间,整理好自己的答题技巧库,诸如此类的题要在最短的时间做出选择。
君翰教育高中化学一对一辅导复习资料今天暂时到这,后面会根据班课反应情况,继续为正在备考的学生分享答题技巧和解题思路。
更多关于高中化学辅导请关注
君翰教育官方网站:www.junhanedu.com
君翰教育高中化学辅导电话:400-8940-050








